„Cink-oxid” változatai közötti eltérés
| [ellenőrzött változat] | [ellenőrzött változat] |
a kis kieg (infobox) |
a r2.7.1) (Bot: következő hozzáadása: da:Zinkoxid |
||
| 75. sor: | 75. sor: | ||
[[cs:Oxid zinečnatý]] |
[[cs:Oxid zinečnatý]] |
||
[[cy:Sinc ocsid]] |
[[cy:Sinc ocsid]] |
||
[[da:Zinkoxid]] |
|||
[[de:Zinkoxid]] |
[[de:Zinkoxid]] |
||
[[el:Οξείδιο του ψευδαργύρου]] |
[[el:Οξείδιο του ψευδαργύρου]] |
||
A lap 2011. március 20., 22:39-kori változata
| Cink-oxid | |
 Cink-oxid | |
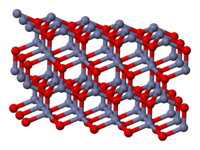
| |
| Más nevek | Horganyfehér |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 1314-13-2 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | ZnO |
| Moláris tömeg | 81,4084 g/mol |
| Megjelenés | Fehér, szilárd |
| Sűrűség | 5,61 g·cm-3 (20 °C)[1] |
| Olvadáspont | 1975 °C[1] |
| Oldhatóság (vízben) | Gyakorlatilag oldhatatlan, 1,6 mg·l (29 °C)-1[1] |
| Termokémia | |
| Std. képződési entalpia ΔfH |
−348,0 kJ/mol |
| Standard moláris entrópia S |
43,9 J·K−1.mol−1 |
| Veszélyek | |
| EU osztályozás | Veszélyes a környezetre (N)[2] |
| NFPA 704 | |
| R mondatok | R50/53[2] |
| S mondatok | S60, S61[2] |
| Rokon vegyületek | |
| Azonos kation | Cink-szulfid Cink-szelenid Cink-tellurid |
| Azonos anion | Kadmium-oxid Higany(II)-oxid |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A cink-oxid (képlete ZnO) a cink oxigénnel alkotott vegyülete, oxidja. Fehér por, kis mértékben sárgás árnyalatú. Hevítés hatására sárga színű lesz, de ha lehűtik, visszanyeri a fehér színét. Vízben gyakorlatilag oldhatatlan, de savakban és erős bázisokban feloldódik, tehát amfoter tulajdonságú. Oldódik nátrium-klorid vizes oldatában is. Nedvszívó hatású, a levegőn szén-dioxidot is elnyel.
Kémiai tulajdonságai
Ha savakban oldódik, cinksókká alakul.
Amfoter vegyület, ugyanis erős bázisok is feloldják, velük szemben gyenge savként viselkedik. Ha bázisokkal reagál, vízben oldódó cinkátokká alakul.
Magasabb hőmérsékleten hidrogén, szén és szén-monoxid hatására cinkké redukálódik. Magasabb hőmérsékleten szintén redukálják az alkálifémek, a magnézium és az alumínium, a reakció heves.
Előfordulása a természetben
A természetben a vörös cinkérc vagy cinkit ásványként fordul elő. Ez hatszöges kristályokat alkot. Vörös színét az okozza, hogy mangánt tartalmaz.
Előállítása
Ha a cinket a levegőn elégetik, finom fehér porként cink-oxid keletkezik.
Előállítható cink-szulfátból is, úgy, hogy az oldatához nátrium-karbonátot adnak, és ezzel az oldatból cink-karbonát csapadékot választanak le. A csapadékot kimossák, majd izzítják, hogy cink-oxiddá alakuljon.
Felhasználása
A cink-oxidot olajfestékekben használják horganyfehér néven. Jó a fedőképessége. Felhasználják cinksók előállítására is. A cink-oxalát hevítésével előállított cink-oxidot katalizátorként alkalmazzák a szén-monoxidból és hidrogénből kiinduló metanolgyártásnál. Hintőporként használják a kozmetikában. Az orvosi gyakorlatban cinkkenőcsként és ragtapaszként alkalmazzák.
Források
- Erdey-Grúz Tibor: Vegyszerismeret
- Nyilasi János: Szervetlen kémia
Hivatkozások
- ↑ a b c A cink-oxid vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2011. 01. 17. (JavaScript szükséges) (angolul)
- ↑ a b c A cink-oxid veszélyei (ESIS)



