„Salétromsav” változatai közötti eltérés
| [nem ellenőrzött változat] | [nem ellenőrzött változat] |
a Robot: Kiskötőjel cseréje gondolatjelre |
a linkcsere |
||
| 35. sor: | 35. sor: | ||
{{chemical_compound_end}} |
{{chemical_compound_end}} |
||
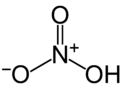
A '''salétromsav''' (régi nevei: ''légenysav'', ''választóvíz'') egy [[nitrogén]] alapú egybázisú [[sav]]. [[Vegyi képlet]]e: |
A '''salétromsav''' (régi nevei: ''légenysav'', ''választóvíz'') egy [[nitrogén]] alapú egybázisú [[sav]]. [[Vegyi képlet]]e: [[Hidrogén|H]]{{N}}{{O}}<sub>3</sub>. |
||
==Felfedezése== |
==Felfedezése== |
||
A lap 2007. június 5., 19:17-kori változata
| Ez a szócikk részben vagy egészben a Pallas nagy lexikonából való, ezért szövege és/vagy tartalma elavult lehet.
Segíts nekünk korszerű szócikké alakításában, majd távolítsd el ezt a sablont! |
| Salétromsav | |
|---|---|
| |
| Általános | |
| Magyar név | Salétromsav |
| IUPAC név | Nitric acid |
| Egyéb nevek | Választóvíz |
| Képlet | |
| Moláris tömeg | 63,01 g/mol |
| Megjelenés | Színtelen, enyhén sárgás, füstölgő folyadék |
| CAS-szám | [7697-37-2] |
| EINECS (EG) szám | – |
| EG-Index szám | 007-004-00-1 |
| Tulajdonságok | |
| Sűrűség és halmazállapot | 1,37 g/cm3, folyadék |
| Oldhatóság vízben | Korlátlanul elegyedik |
| Olvadáspont | −22 °C (251 K) |
| Forráspont | ~120 °C (~393 K) |
| Szerkezet | |
| Kristályszerkezet | - |
| Fizikai állandók | |
| Képződéshő | - kJ/mol |
| Moláris hőkapacitás | - J/(mol·K) |
| Veszélyességi jellemzők | |
| EU osztályozás | Maró (C) |
| R-mondatok | R35 |
| S-mondatok | S23, S26, S36/37/39, S45 |
| Lobbanáspont | |
| RTECS szám | - |
| Rokon vegyületek | |
| Azonos anion | Nitrátok |
| Azonos kation | |
| A táblázatban SI mértékegységek szerepelnek. Ahol lehetséges, az adatok normálállapotra (0°C, 100 kPa) vonatkoznak. Az ezektől való eltérést egyértelműen jelezzük. | |
A salétromsav (régi nevei: légenysav, választóvíz) egy nitrogén alapú egybázisú sav. Vegyi képlete: HSablon:N![]() 3.
3.
Felfedezése
Geber alkimista már a 19. században kálium-nitrát, réz-szulfát és timsó desztillálása útján egy folyadékot készített, melyet aqua dissolutivanak nevezett és amely lényegében salétromsavból állt. Tisztán a legnagyobb valószínűséggel legelőször Glauber állította elő. A természetben szabad állapotban sehol sem található, de sói (nitrátok) meglehetősen el vannak terjedve, mert folytonosan képződnek a talajban, sőt egyes helyeken (a nátrium-nitrát Peruban) nagyobb mennyiségben is találhatók.
Képződése
A salétromsav sokféle módon képződik, így pl. mikor nedves nitrogén és oxigén elegyén (levegőn) elektromos szikra ugrik át; mikor hidrogént levegővel és oxigénnel keverve eldurrantunk, vagy ha hidrogénlángot oxigénnel kevert levegőbe mártunk; úgyszintén, ha ammóniagázt oxigénben elégetünk.
Gyártása
Előállítása rendszerint úgy történik, hogy kálium-vagy nátrium-nitrátot retortában tömény kénsavval melegítenek, amikor a lehűtött szedőbe salétromsav párolog át. Minthogy azonban a salétromsav már 86 °C-on (forráspontján) nitrogén-tetroxid elbomlik, egészen tiszta salétromsavat csak úgy kaphatunk, ha a lepárlást légritkított térben végezzük. A tiszta sav színtelen, a kereskedésben található (legfeljebb 68%-os) ellenben sárgás vagy vörössárga színű (acidum nitricum fumans) a szerint, amint kevesebb vagy több nitrogén-tetroxid van benne.
Az oldat fajsúlya a töménységgel arányosan növekszik:
| Savtartalom (%) | Fajsúly (kg/l) |
| 5 | 1,029 |
| 10 | 1,060 |
| 20 | 1,120 |
| 30 | 1,185 |
| 40 | 1,251 |
| 50 | 1,317 |
| 60 | 1,347 |
| 58 | 1,414 |
| 70 | 1,423 |
| 80 | 1,460 |
| 90 | 1,495 |
| 100 | 1,530 |
Biológiai hatásai
A koncentrált salétromsav a levegőn füstölög, gőze sajátságos szagú és belehelve erősen maró. Magasabb hőmérsékleten vízre, nitrogén-tetroxidra és oxigénre bomlik, hasonlóan bomlik el a világosságon is, ezért a legtisztább salétromsav is lassankint megsárgul.
Egyike a legerélyesebb oxidáló szereknek, olyannyira, hogy a tiszta koncentrált salétromsavba mártott parázs lángra lobban, és a tömény borszesz meg a terpentinolaj lángra lobbannak. A platinacsoport és az arany kivételével, feloldja és salétromsav-sókká (nitrátokká) alakítja át a fémeket. A széntartalmú vegyületeket szintén oxidálja vagy nitrovegyületekké alakítja át. A bőrt annyira megtámadja, hogy a felhám elhal és kevés idő múlva lehámlik.
Felhasználása
A salétromsavat főleg sóinak előállítására, a lőgyapot, nitroglicerin gyártására, az aranynak más fémektől való elválasztására (ezért hívják választóvíznek) és az orvosi gyakorlatban inficiált sebek kimosására használják. A magyar a gyógyszerkönyvben hivatalos. Elvárás, hogy kloridokkal, szulfátokkal, rézzel, ólommal ne legyen szennyezve. A salétromsav és a sói is könnyen felismerhetők koncentrált kénsavban oldott difenilaminnal, amellyel szép sötétkék színű vegyületet képez.
Irodalom
Jegyzetek

