Piridazin
| Piridazin | |||
| |||
 C=fekete, H=fehér, N=kék |
 C=fekete, H=fehér, N=kék | ||
| Más nevek | 1,2-diazin ortodiazin oizin | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 289-80-5 | ||
| PubChem | 9259 | ||
| ChemSpider | 8902 | ||
| EINECS-szám | 206-025-5 | ||
| ChEBI | 30954 | ||
| RTECS szám | GY2390000 | ||
| |||
| |||
| InChIKey | PBMFSQRYOILNGV-UHFFFAOYSA-N | ||
| ChEMBL | 15719 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C4H4N2 | ||
| Moláris tömeg | 80,09 g/mol | ||
| Megjelenés | színtelen folyadék | ||
| Sűrűség | 1,107 g/cm³ | ||
| Olvadáspont | −8 °C | ||
| Forráspont | 208 °C | ||
| Oldhatóság (vízben) | elegyedik | ||
| Oldhatóság | elegyedik dioxánnal, etanollal oldódik benzolban, dietil-éterben elhanyagolható mértékben oldódik ciklohexánban, lakkbenzinben | ||
| Törésmutató (nD) | 1,52311 (23,5 °C) | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH |
224,9 kJ/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
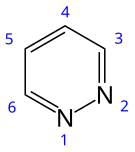
A piridazin aromás heterociklusos szerves vegyület, képlete (CH)4N2. Hattagú gyűrűjében két szomszédos nitrogénatom található.[1] Színtelen folyadék, forráspontja 208 °C. Két – (CH)4N2 képletű –, vele izomer gyűrűs vegyület a pirimidin és a pirazin.
Előfordulása[szerkesztés]
Piridazinok a természetben ritkán fordulnak elő, ez talán annak köszönhető, hogy ezen heterociklusok szokásos szintetikus építőelemei, a hidrazinok is ritkaságszámba mennek a természetben. A piridazinszerkezet népszerű farmakofór, mely számos herbicidben előfordul, ilyen például a kredazin, a piridafol és a piridát. Megtalálható továbbá több gyógyszermolekula, például a cefozoprán, cadralazin, minaprin, pipofezin és hidralazin szerkezetében is.
Szintézise[szerkesztés]
Az első piridazint Emil Fischer állította elő az indolszintézis klasszikus vizsgálata közben, fenilhidrazin és levulinsav kondenzációja révén.[2] Az alap heterociklusos vegyületet először benzocinnolin piridazintetrakarbonsavvá történő oxidációja, majd azt követő dekarboxilezéssel állították elő. Ezen – egyébként egzotikus – vegyület előállításának jobb módja a maleinsav-hidazidból kiindulő szintézis. Ezeket a heterociklusokat gyakran 1,4-diketon vagy 4-ketosav és hidrazin közötti kondenzációval állítják elő.[3]
Jegyzetek[szerkesztés]
- ↑ (2011) „A computational study on substituted diazabenzenes” (PDF). Turk J Chem 35, 803–808. o. [2016. március 3-i dátummal az eredetiből archiválva]. (Hozzáférés: 2019. március 27.)
- ↑ (1886) „Indole aus Phenylhydrazin”. Justus Liebigs Annalen der Chemie 236 (1-2), 126–151. o. DOI:10.1002/jlac.18862360107.
- ↑ (1968) „Pyridazines”. Advances in Heterocyclic Chemistry 9, 211–320. o. DOI:10.1016/S0065-2725(08)60374-8.
Fordítás[szerkesztés]
- Ez a szócikk részben vagy egészben a Pyridazine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
